N 元反应速率理论(卷名:化学)
N-elementary reactionrate theory
在一定的模型假定下应用统计热力学、经典力学和量子力学等来研究元反应速率的理论,它包括简单碰撞理论、量子力学的碰撞理论和过渡态理论。知道了一个复杂反应中各个元反应的速率,就能知道该复杂反应的速率,从而把研究化学反应速率的问题归结为研究各元反应速率的问题。
简单碰撞理论 两个分子必须碰到一起(称为两个分子发生了碰撞),然后才能起化学反应。一个分子在一秒钟内同其他分子碰撞的次数称为碰撞频率。简单碰撞理论认为,相碰分子的总动能必须大于某个值才会发生化学反应。分子碰撞而能发生化学反应的最小动能称为临界能Ec,Ec随碰撞分子而异。一立方厘米体积中,两个分子在一秒钟内相碰撞的次数称为碰撞速率。能够发生化学反应的碰撞称为有效碰撞。分子碰撞理论认为,化学反应的速率等于有效碰撞速率。
假设分子为刚球,分子A的半径为rA,分子B的半径为rB,每立方厘米内有nA个A分子和nB个B分子,分子A对分子B的平均相对速度为婔,则A分子同B分子的碰撞速率ZAB为:
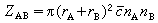 此式是出于如下考虑得到的,即以rA+rB为半径的圆面在一秒钟内运动所扫过的体积为π(rA+rB)2婔,在此体积内分子A的数目为 π(rA+rB)2婔nA,它们都能分别与该体积中的一个分子B碰撞。π(rA+rB)2婔nA为分子B的碰撞频率,将它乘以分子B 的密度nB就得到碰撞速率ZAB。相碰撞分子的总动能有大有小,总动能E超过Ec的碰撞,才能起化学反应,这相当于以下假定:
此式是出于如下考虑得到的,即以rA+rB为半径的圆面在一秒钟内运动所扫过的体积为π(rA+rB)2婔,在此体积内分子A的数目为 π(rA+rB)2婔nA,它们都能分别与该体积中的一个分子B碰撞。π(rA+rB)2婔nA为分子B的碰撞频率,将它乘以分子B 的密度nB就得到碰撞速率ZAB。相碰撞分子的总动能有大有小,总动能E超过Ec的碰撞,才能起化学反应,这相当于以下假定:
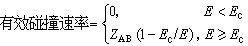 根据玻耳兹曼分布率,可得平均有效碰撞速率为:
根据玻耳兹曼分布率,可得平均有效碰撞速率为:
(墫AB)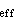 =ZABexp(-Ec/RT)
=ZABexp(-Ec/RT)
如果分子A和分子B是同种分子,则如上算得的碰撞速率应除以2,因为对于同种分子,上述计数实际重复了两次。
分子不是球型的,更不是刚球,所以两个分子碰撞是否有效,还须看碰撞的方位如何。例如,氢原子同氟化氢分子的碰撞,可分为两种方位:
H+HF─→H2+F
H+FH─→HF+H对于生成氢分子来说,只有前一种碰撞有效,所以真正的平均有效碰撞速率是上述平均有效碰撞速率乘以一个小于1的因子P:
(墫AB)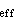 =PZABexp(-Ec/RT)式中P为方位因子。
=PZABexp(-Ec/RT)式中P为方位因子。
反应速率常数k等于分子浓度为1单位时的有效碰撞速率:
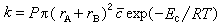 因为
因为 ,它与绝对温度T 有关,而S.A.阿伦尼乌斯提出的指数定律(见活化能)的指前因子A 与温度无关,所以Ec不等于活化能。
,它与绝对温度T 有关,而S.A.阿伦尼乌斯提出的指数定律(见活化能)的指前因子A 与温度无关,所以Ec不等于活化能。
量子力学的碰撞理论 分子起化学反应,是分子中的电子和原子核相互作用和运动的结果,例如以下双分子元反应:
A+B─→C+D分子A和分子B由彼此相距很远,运动至相距很近,以至碰撞,从而分子A中的电子同分子B中的电子和原子核相互作用,分子相距越近,相互作用越强。这种相互作用改变电子和原子核的结合对象,使原来的分子分解,生成新分子。
电子的质量比原子核的质量小很多,运动比原子核快得多。电子运动一周,原子核基本未动。因此,原子核是在电子的平均力作用下运动的,该力决定着原子核运动所受的势能,它是原子核间距的函数,称为势能函数。如果势能函数只是两个独立核间距的函数,则以两个核间距为纵横坐标对势能函数作图,得到一个真正的曲面,称为势能面。如果势能函数是三个以上独立核间距的函数,将势能函数对独立核间距作图,则得到广义的曲面,称为超势能面。
当原子与双原子分子起反应,且三个原子在一条直线上运动时,势能函数只是两个独立变量的函数,例如共线反应(图1):
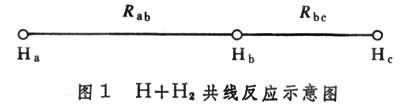
Ha+Hb-Hc─→Ha-Hb+Hc势能函数是两个独立变量核间距Rab和Rbc的函数。
图2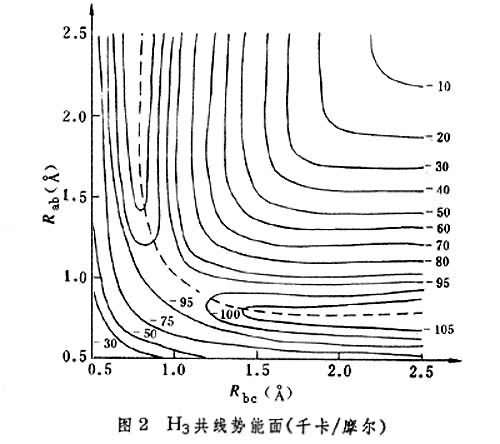 是H3的共线势能面,当Rab趋于∞时,H3成为反应物分子,等于Ha+Hb─Hc;当Rbc趋于∞时,则H3成为产物分子,等于Ha─Hb+Hc。图中的曲线是势能等值线,即在此曲线上,势能值是相等的。此图很像一幅山区地图,在两边陡峭的山间有一条小路,称为最小能途径,因为它是能量最低点的联线。
是H3的共线势能面,当Rab趋于∞时,H3成为反应物分子,等于Ha+Hb─Hc;当Rbc趋于∞时,则H3成为产物分子,等于Ha─Hb+Hc。图中的曲线是势能等值线,即在此曲线上,势能值是相等的。此图很像一幅山区地图,在两边陡峭的山间有一条小路,称为最小能途径,因为它是能量最低点的联线。
在反应物区和产物区的最小能途径之间有一小的凸起区,称为势垒,势垒的顶点称为鞍点,此处的势能图呈马鞍形。沿最小能途径走向反应物区和产物区,势能均急剧下降;沿着最小能途径的垂直方向,则势能急剧上升。反应开始时,基态反应分子越过势垒所需的最小动能(E0称为阈值能)。反应分子的总能量(以反应开始时的基态内能为标准)必须高于E0,反应才能发生。
按照反应势垒出现的位置,势能面可分为三种:①势垒在最小能途径的对称位置上。这类反应的势能面对反应区和产物区是对称的,即反应物和产物的性质相同。例如 H+H2─→H2+H,属于这类反应。②势垒在反应区,F+H2─→HF+H反应属于此类(图3)。这类势垒称为早期势垒。③势垒在产物区,上述反应的逆反应属于此类,其势垒称为晚期势垒。

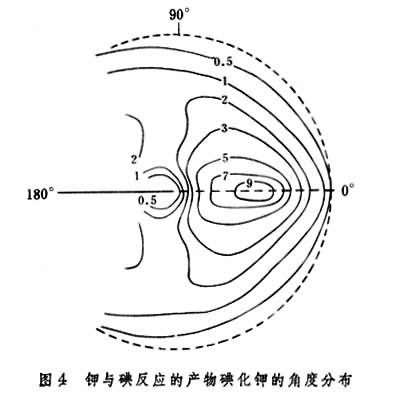
 按照势垒的不同结构,势能面又可分为两类:①势垒顶没有浅洼,这种反应称为直接反应,其产物的角度分布在前后方向上是不同的(图4);②势垒顶上有浅洼,此种反应称为间接反应,其产物在前后方向上的分布基本相同(图5)。
按照势垒的不同结构,势能面又可分为两类:①势垒顶没有浅洼,这种反应称为直接反应,其产物的角度分布在前后方向上是不同的(图4);②势垒顶上有浅洼,此种反应称为间接反应,其产物在前后方向上的分布基本相同(图5)。
反应坐标可用来表示反应进行的程度。图6 示出反应物和产物分子的势能随反应坐标的变化。反应坐标是化学键生成和分解程度的度量,在势垒顶及其附近,反应坐标同势能面和超势能面的最小能途径一致。
示出反应物和产物分子的势能随反应坐标的变化。反应坐标是化学键生成和分解程度的度量,在势垒顶及其附近,反应坐标同势能面和超势能面的最小能途径一致。
如果势能是三个以上独立坐标的函数,则不能用一张图表示出势能随坐标的变化,须用一系列的图才能表达。每张图都是选定两个独立坐标而固定其他坐标画出的势能等值图。图7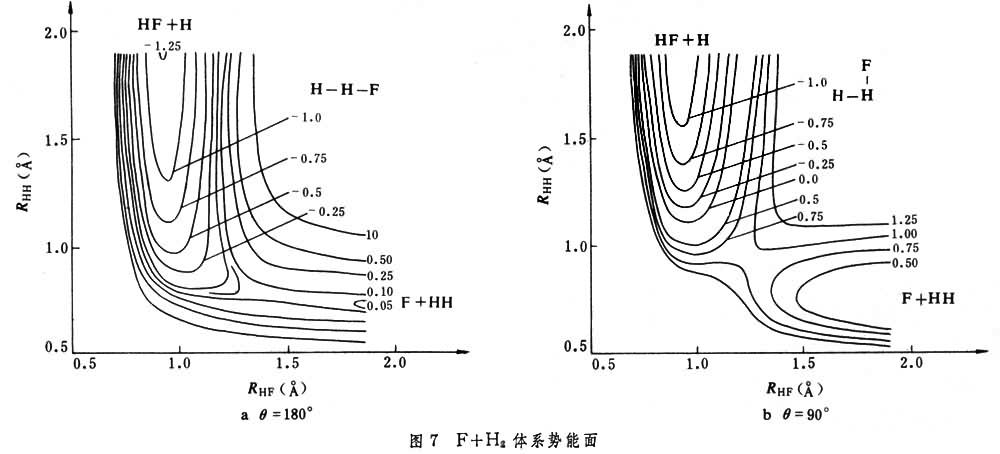 是固定夹角的势能面图。另一种是固定双原子分子的键长,对夹角和一个核间距画出的势能面图,但这种势能面图不常应用。
是固定夹角的势能面图。另一种是固定双原子分子的键长,对夹角和一个核间距画出的势能面图,但这种势能面图不常应用。
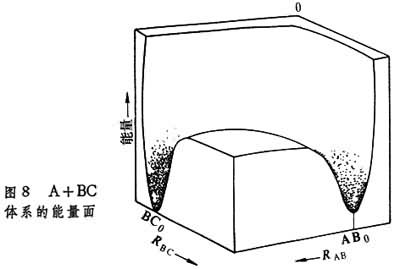
上面的势能面是在二维平面上用等直线标明势能值大小而画出的,这是最常用的势能面图。有时用三维坐标直接画出势能的大小。但因为核间距是自0→∞,所以为了便于了解,只截出核间距为某一定值的图(图8)。
 过渡态理论 在势能面的反应途径上存在势垒,这是大多数元反应的共同性质。只有极快速的元反应才不存在势垒。对于直接反应,势垒顶峰没有浅洼,在其顶峰处的反应分子称为过渡态。对于间接反应,反应物与络合物以及络合物与产物之间均会存在势垒。势垒顶峰处的反应分子或产物分子都可以称为过渡态,例如原子A同分子BC的直接反应:
过渡态理论 在势能面的反应途径上存在势垒,这是大多数元反应的共同性质。只有极快速的元反应才不存在势垒。对于直接反应,势垒顶峰没有浅洼,在其顶峰处的反应分子称为过渡态。对于间接反应,反应物与络合物以及络合物与产物之间均会存在势垒。势垒顶峰处的反应分子或产物分子都可以称为过渡态,例如原子A同分子BC的直接反应:
A+BC─→(ABC)≠─→AB+C式中(ABC)≠表示过渡态(凡与过渡态有关的物理量都标有“≠”)。
过渡态的特征是:①有一定的几何构型,AB和BC的核间距均较小,但大于这两个双原子分子的键长;②能量不小于阈值能E0;③构型不稳定,寿命短于一皮秒。过渡态理论假设:①元反应均经过过渡态;②过渡态是不返回态,即过渡态只朝向产物分解,不回到反应物中去;③过渡态处于热平衡中,在这些假设下,过渡态就像通常分子一样,可用统计热力学讨论。
根据过渡态的假设,并假定过渡态与反应物达到化学平衡,可推导出元反应的速率公式,也称艾林公式:
 式中k为反应速率常数;R为气体常数;T为热力学温度;h为普朗克常数;噕v为透过系数;Q为配分函数;N为阿伏伽德罗数。
式中k为反应速率常数;R为气体常数;T为热力学温度;h为普朗克常数;噕v为透过系数;Q为配分函数;N为阿伏伽德罗数。
放弃过渡态同反应物达到化学平衡的假设,由量子力学(或经典力学)和统计力学可以更严格地推导出反应速率的表达式,它的形式与艾林公式相同。由配分函数可以写出过渡态和反应物的平衡常数K≠:
 因此,反应速率常数k为:
因此,反应速率常数k为:
 根据统计热力学,活化吉布斯函数ΔG≠是过渡态吉布斯函数G≠与反应物吉布斯函数Gr之差:
根据统计热力学,活化吉布斯函数ΔG≠是过渡态吉布斯函数G≠与反应物吉布斯函数Gr之差:
 式中H≠为过渡态焓;Hr为反应物焓;S≠为过渡态熵;Sr为反应物熵;ΔH≠为活化热焓,ΔS≠为活化熵。反应速率常数k可表示为:
式中H≠为过渡态焓;Hr为反应物焓;S≠为过渡态熵;Sr为反应物熵;ΔH≠为活化热焓,ΔS≠为活化熵。反应速率常数k可表示为:
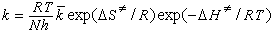 由活化吉布斯函数ΔG≠可得到活化体积ΔV≠:
由活化吉布斯函数ΔG≠可得到活化体积ΔV≠:
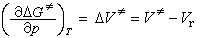 活化体积是过渡态摩尔体积 V≠与反应物摩尔体积Vr之差。由活化吉布斯函数与K≠的关系以及K≠与反应速率常数的关系可得:
活化体积是过渡态摩尔体积 V≠与反应物摩尔体积Vr之差。由活化吉布斯函数与K≠的关系以及K≠与反应速率常数的关系可得:
 利用活化热力学函数,反应速率常数公式可以推广应用于液相化学反应。
利用活化热力学函数,反应速率常数公式可以推广应用于液相化学反应。