理想气体状态方程(卷名:物理学)
equation of state of ideal gas
描写理想气体状态变化规律的方程。对于一定质量的气体,可以用压强p和体积V来描述它的平衡态,而温度T是p和V的函数,F(T,p,V)=0。这个关系式叫做气体的状态方程,它的具体形式需由实验确定。
玻意耳定律 又称玻意耳—马略特定律,是英国化学家R.玻意耳在1662年和法国物理学家E.马略特在1679年分别独立发现的。它的内容是:一定质量的气体,当温度保持不变时,压强和体积成反比且乘积是一个常数
p1V1=p2V2=p3V3=…或pV=C。常数C 在不同温度时有不同数值。
大量实验结果表明,该定律对理想气体完全正确。对于各种实际气体,只要它的压强不太高,温度不太低,都近似地遵从此定律;气体的压强越低,它遵从玻意耳定律的精确度就越高。
盖-吕萨克定律 一定质量的气体,当体积不变时,它的压强随温度作线性变化:
p=p0(1+αt),p0是0°C时的气体压强,p是t°C时的气体压强,α是在气体体积不变时的压强系数。对于理想气体,α的数值为一普适常数,其值为1/273.15,于是
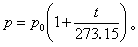 若令T=t+273.15,则上式简化为
若令T=t+273.15,则上式简化为pt=p0αT,T 即为热力学温标,其单位是开尔文 (K);t=0时,T0=273.15K。
理想气体状态方程 根据玻意耳定律、阿伏伽德罗定律和理想气体温标的定义,可以确定玻意耳定律中常数C与温度的关系,并可导出
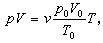 式中p0、V0、T0为标准状况下一摩尔理想气体的压强、体积、温度;v为摩尔数。因此,
式中p0、V0、T0为标准状况下一摩尔理想气体的压强、体积、温度;v为摩尔数。因此,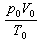 的数值对各种气体都一样。该数值叫摩尔气体常数并用r表示:
的数值对各种气体都一样。该数值叫摩尔气体常数并用r表示: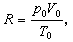 于是
于是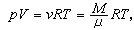 式中M代表气体的质量,μ 是气体的分子量。这就是理想气体状态方程。
式中M代表气体的质量,μ 是气体的分子量。这就是理想气体状态方程。在压强为几个大气压以下时,各种实际气体一般都近似地遵从理想气体状态方程。压强越低,符合的程度越高。在压强趋于零的极限情况下,一切气体都严格地遵从它。根据理想气体模型,从气体分子运动论出发,也可以推导出该物态方程。
摩尔气体常数R R的数值可由一摩尔理想气体在水的三相点 (273.16K)及一个大气压下的体积推出。也可以由一摩尔理想气体在冰点 (273.15K)及一个大气压下的体积V0推出。用V0来推算的原因是 V0可根据实验结果求得比较准确的数值。由
V0=22.41383×10-3m3/mol可算得
r=8.31441±0.00026J/(mol·K)。