钾(卷名:化学)
potassium
一种化学元素,化学符号 K,原子序数19,原子量39.098 3,属周期系IA族,为常见的碱金属元素之一。
发现 1807年英国化学家H.戴维首次用电解法从氢氧化钾熔体中制得金属钾,并定名。元素英文名potas-sium来源于potash(草木灰),化学符号来源于拉丁文Kalium,原意是“碱”。
存在 钾在地壳中的含量是2.59%,在所有元素中居第 7位。重要的钾矿物有钾石盐、钾硝石、光卤石和钾铝钒等。海水中也含氯化钾,其含量为氯化钠的1/40。土壤中的钾很容易进入植物组织,所以植物灰中都含碳酸钾。钾有三种天然同位素,即钾39、钾40和钾41。
物理性质 钾是一种轻而软的低熔点金属;熔点为63.25℃,沸点760℃,密度0.86克/厘米3(20℃)。
化学性质 钾的电子构型为(Ar)4s1,氧化态为+1、-1。钾比钠活泼,金属钾与水或冰的反应,即使温度低到-100℃也非常剧烈。金属钾与酸的水溶液反应更为剧烈。金属钾在空气中燃烧,或与1大气压的氧气作用,都易生成橘红色的超氧化钾 KO2,超氧化钾又易发生下述反应:
4KO2+2H2O+4CO2─→4KHCO3+3O2释放出氧气,可在呼吸面罩中作供氧剂。金属钾与氨反应生成氨基化钾:
2K+2NH3─→2KNH2+H2在200℃时,金属钾与氢气反应很慢,但在400℃时反应很快。金属钾与一氧化碳反应能生成一种爆炸性的羰基化合物。
钾能使火焰呈现紫色,由于经常有钠共存,在定性观察时可用钴玻璃把钠焰的黄色滤掉。
制法 钾可用金属钠还原熔融的氯化钾来制取:
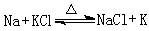
应用 金属钾可制成钠-钾合金 NaK,其熔点只有-12.5℃,它能象液钠一样传热,但不易固化,在增殖反应堆中作热交换剂。钾盐是重要的肥料,是植物生长的三大营养元素之一。