热力状态参数(卷名:机械工程)
parameters of thermodynamic state
描写热力状态的物理量,简称状态参数。热力学中常用的状态参数有压力、比容、温度、内能、焓、熵、亥姆霍兹函数和吉布斯函数等。
压力 单位面积上承受的垂直作用力,以符号p表示。压力测量仪表通常处于大气环境中,因此仪表指示的并非气体的真实压力而是它与大气压力
 的差值。气体的真实压力称为绝对压力。当绝对压力高于大气压力时,压力测量仪表所指示的是绝对压力超出大气压力的部分,称为表压力(p0):p0=p-
的差值。气体的真实压力称为绝对压力。当绝对压力高于大气压力时,压力测量仪表所指示的是绝对压力超出大气压力的部分,称为表压力(p0):p0=p- 。当气体的绝对压力低于大气压力时,真空计所指示的是绝对压力低于大气压力的部分,称为真空度(pv):pv=
。当气体的绝对压力低于大气压力时,真空计所指示的是绝对压力低于大气压力的部分,称为真空度(pv):pv= -p。在国际单位制中,压力的单位是帕〔Pa〕。
-p。在国际单位制中,压力的单位是帕〔Pa〕。比容 单位质量物质所占有的容积。若 m质量的物质占有V 容积,则比容为:v=V/m。比容的倒数称为密度
 ,是单位容积的物质所具有的质量,即
,是单位容积的物质所具有的质量,即 =m/V=1/v。
=m/V=1/v。温度 表示物体的冷热程度。热力学中的温度是衡量一个热力系统是否与其他热力系统处于热平衡的标志,一切处于热平衡的系统都具有相同的温度。对于气体,温度是大量气体分子平均移动动能的量度,即
 式中m为分子的质量;堹为分子平移均方根速度;k为玻耳兹曼常数;T 为热力学温度。
式中m为分子的质量;堹为分子平移均方根速度;k为玻耳兹曼常数;T 为热力学温度。温度的数值表示法,称为温度标尺或"温标"。在国际单位制中采用热力学温标,也就是采用开尔文温标或绝对温标,用符号T表示,单位是K。规定水的三相点(冰、水、汽三相平衡共存时的状态)为273.16K,每1K的间隔为水的三相点热力学温度的1/273.16。此外,常用的还有摄氏温标和华氏温标。摄氏温标符号为t,定义为
t(℃)=T(K)-273.15
摄氏温标的单位是摄氏度,符号℃,其每度间隔与热力学温标的相同。华氏温标 t则将水在 1标准大气压(101325帕)时的冰点和汽点分别定为32度和212度,中间为180分度,单位是
 ,它与摄氏温标之间的换算关系为
,它与摄氏温标之间的换算关系为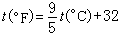 用华氏温标表示的热力学温标称为兰金温标 (Rankine scale)或称热力学华氏温标,也用符号T 表示,单位是
用华氏温标表示的热力学温标称为兰金温标 (Rankine scale)或称热力学华氏温标,也用符号T 表示,单位是 ,它们之间的换算关系为
,它们之间的换算关系为T(
 )=t(
)=t(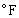 )+459.67
)+459.67内能 从微观看,内能是指组成热力系统的大量粒子本身所具有的能量,包括分子的动能、位能、化学能和原子的核能等。在发生物理变化时,物质的分子和原子内部结构都不发生变化,化学能与原子的核能可以不必考虑。这时可以用p、v、T 中的任意两个状态参数来确定它的状态。对于理想气体,内能只与温度有关。单位质量的内能称为比内能。内能和比内能分别用符号U 、u表示。
焓 焓的定义式为
H=U +pV焓的单位为焦耳(J)。单位物质的焓称为比焓,它表示为
h=u+pv比焓的单位为焦每千克(J/kg)。
熵 熵的微分定义式为
 它表示系统的熵增等于在可逆过程中该系统与外界交换的热量δQ同系统的热力学温度T的比值。式中S为热力系统的熵 (J/K),它是由热力学第二定律导出的状态参数。单位质量的熵称为比熵,单位为焦每千克开〔J/(kg·K)〕,它表示为熵除以质量,即s=S/m。
它表示系统的熵增等于在可逆过程中该系统与外界交换的热量δQ同系统的热力学温度T的比值。式中S为热力系统的熵 (J/K),它是由热力学第二定律导出的状态参数。单位质量的熵称为比熵,单位为焦每千克开〔J/(kg·K)〕,它表示为熵除以质量,即s=S/m。亥姆霍兹函数 又称亥姆霍兹自由能或定温-定容位,定义式为:F=U-TS。单位质量的亥姆霍兹函数定义为:f=u-Ts。是定温-定容条件下,可利用热力系统F(或f)值的变化来判断过程自发进行的方向和限度。
吉布斯函数 又称吉布斯自由能或定温-定压位,定义式为:G=H-TS。单位质量的吉布斯函数定义为:g=h-Ts。在定温-定压条件下,可利用热力系统G(或g)值的变化来判断过程自发进行的方向和限度。