溶液中离子的扩散(卷名:化学)
ionic diffusion in solution
扩散是溶液的基本性质,是微粒(分子、原子)的热运动而产生的物质迁移现象,主要由浓差、温差和湍流运动引起,研究扩散可为溶液结构提供信息。
液体扩散的基本公式是斐克定律:
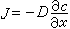 式中J为物质的通量,即单位时间内通过单位面积的物质量;D是扩散系数;
式中J为物质的通量,即单位时间内通过单位面积的物质量;D是扩散系数;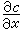 是浓度梯度。
是浓度梯度。电解质溶液的扩散 两组分体系中的扩散 在单组分体系中,自扩散系数用D*表示;在两组分体系中用D奮和D奯表示。在非理想情况下,D奯为浓度的函数,如果忽略粘度η对淌度U的影响,则有:
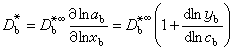 式中D凁为c →0时的D奯;ab为活度;cb为浓度;xb为摩尔分数;yb为摩尔活度系数。由于组分i的淌度 Ui是单位力影响下组分i所获得的平均漂移速度,或简单地认为是摩擦系数f的倒数,根据斯托克斯定律f=6πηr(r为粒子半径),则U与1/η成正比,在考虑η变化时,上式可写成:
式中D凁为c →0时的D奯;ab为活度;cb为浓度;xb为摩尔分数;yb为摩尔活度系数。由于组分i的淌度 Ui是单位力影响下组分i所获得的平均漂移速度,或简单地认为是摩擦系数f的倒数,根据斯托克斯定律f=6πηr(r为粒子半径),则U与1/η成正比,在考虑η变化时,上式可写成: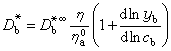 式中
式中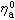 为纯组分a的粘度。
为纯组分a的粘度。单电解质的扩散 在电解质溶液中,极限当量电导
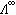 与扩散系数D+、D_之间的关系可用能斯脱-爱因斯坦公式表达:
与扩散系数D+、D_之间的关系可用能斯脱-爱因斯坦公式表达: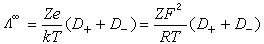 式中Z为离子的电荷数;e为电子的电荷数;k为玻耳兹曼常数;T为热力学温度;F为法拉第常数;R为气体常数。当c→0时,上式可简化为:
式中Z为离子的电荷数;e为电子的电荷数;k为玻耳兹曼常数;T为热力学温度;F为法拉第常数;R为气体常数。当c→0时,上式可简化为: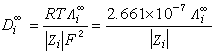
在电解质溶液中,电中性要求正、负离子都以同样的速率移动,因此,对于电解质从整体上说存在着一个扩散系数Db。在x方向的某一离子的扩散速度ui为:
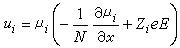 式中
式中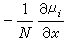 为粒子i在x方向的驱动力;μi为粒子i的化学势;N 为阿伏加德罗数;ZieE为在电场E的存在下,带电荷Zie的离子i遭受到的力。对于正和负离子,这个扩散速度都应该是同样的,从式 u+=u-消除E,并应用v+Z++v-Z-=0的关系,可得:
为粒子i在x方向的驱动力;μi为粒子i的化学势;N 为阿伏加德罗数;ZieE为在电场E的存在下,带电荷Zie的离子i遭受到的力。对于正和负离子,这个扩散速度都应该是同样的,从式 u+=u-消除E,并应用v+Z++v-Z-=0的关系,可得: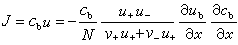 式中J为溶质通量;v+和v-为正负离子个数。将上式与斐克定律相比,得:
式中J为溶质通量;v+和v-为正负离子个数。将上式与斐克定律相比,得: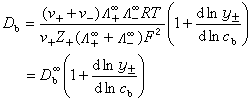 式中y±为平均体积摩尔活度系数,此式称为能斯脱-哈脱莱方程。
式中y±为平均体积摩尔活度系数,此式称为能斯脱-哈脱莱方程。电泳效应对扩散的影响 在电导中,离子互相吸引产生两种效应:一是松弛效应,即外电场的影响使对称的离子氛转化为非对称的;另一种是电泳效应,即在外电场的影响下溶剂分子和离子作反向的对流。在单独电解质的扩散里,两种离子以相同速率向前推进,离子氛的对称性仍能维持,因而没有松弛效应,但是电泳效应仍然存在,因为离子移动时穿过溶剂,而溶剂分子的扩散方向是相反的。这个效应与电解质的浓度有关,对称电解质从无限稀到浓度c时,可得到:
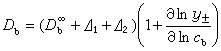 这些效应引起Db的改正为墹1+墹2,它只有电导率相应的改正值的1/10。
这些效应引起Db的改正为墹1+墹2,它只有电导率相应的改正值的1/10。缔合式电解质对扩散的影响 离子缔合对扩散的影响是降低微粒的阻力。因为在液体中移动时,一个微粒的阻力总比两个小些,结果扩散速度上升。在稀溶液中得到下式:
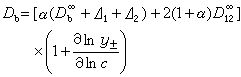 式中 α为电离度;D
式中 α为电离度;D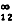 为无限稀释溶液中一个离子对的扩散系数,浓度为0.001~0.005摩尔/千克时D
为无限稀释溶液中一个离子对的扩散系数,浓度为0.001~0.005摩尔/千克时D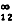 是常数。
是常数。互扩散对扩散的影响 在两组分体系中,当B扩散到右边时,为使体系平衡,必然有一些物质流到左边,因此净效应可被描述为与方向中的整体运动结合的 B的纯扩散。在这种情况下,用单个扩散系数Dab来描述通过扩散的任一组分的浓度变化,就叫做互扩散系数。假设体积与组成无关时,Dab即为:
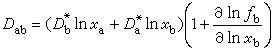 式中xa、xb为组分a、b的摩尔分数;fb为组分b的有理活度系数,此式称为吉布斯-杜亥姆扩散方程,它还可表述为:
式中xa、xb为组分a、b的摩尔分数;fb为组分b的有理活度系数,此式称为吉布斯-杜亥姆扩散方程,它还可表述为: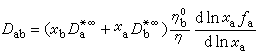 式中已假设u与η成反比关系。
式中已假设u与η成反比关系。自扩散 纯液体分子从一点移动到另一点的运动称为自扩散。在溶液中实际能实现的是示踪扩散,例如极少量的放射性 Na*离子在氯化钠中的扩散。因为 Na*离子的浓度很小,基本无反向溶剂流动,所以电泳效应可以忽略。定量的方程为:
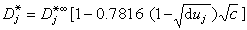 D凂可由能斯脱-爱因斯坦公式计算。
D凂可由能斯脱-爱因斯坦公式计算。浓溶液的扩散 必须考虑溶剂的移动、溶液的粘度和离子的水化。非电解质浓溶液的扩散公式为:
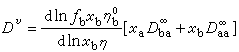 式中xa和xb为溶剂a和溶质b的摩尔分数;D
式中xa和xb为溶剂a和溶质b的摩尔分数;D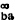 和D
和D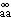 分别为b在无限稀释下的扩散系数和纯溶剂的扩散系数;Dv为两组分体系的分体积不变时的扩散系数。
分别为b在无限稀释下的扩散系数和纯溶剂的扩散系数;Dv为两组分体系的分体积不变时的扩散系数。把上式用于单电解质在浓溶液中的扩散,得出高浓度下水化电解质的扩散公式:
 式中h为电解质水化数。对电解质的体积浓度来说,水化和非水化并无区别,因此Dv即为无水的扩散系数D,
式中h为电解质水化数。对电解质的体积浓度来说,水化和非水化并无区别,因此Dv即为无水的扩散系数D,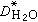 为纯水的扩散系数,对1:1价态的电解质,离子个数v=2。上式能符合许多1:1价态的盐,浓度可达1摩尔/千克,误差约为0.5%。
为纯水的扩散系数,对1:1价态的电解质,离子个数v=2。上式能符合许多1:1价态的盐,浓度可达1摩尔/千克,误差约为0.5%。参考书目
黄子卿:《电解质溶液理论导论》,科学出版社,北京,1964。