能斯脱公式(卷名:化学)
Nernst equation
表示电池电动势和参与电池反应的各种物质的性质、浓度以及外界条件(温度、压力等)的关系式。对任一自发可逆电池,可从热力学导出该电池的电动势E为:
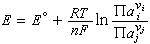 此式由W.H.能斯脱在1889年从热力学导出。式中E°为电池的标准电动势,即参与电池反应物质的活度均为 1时电池的平衡电势或电动势;П为连乘符号;ai和aj分别为电池反应式中反应物一边和生成物一边的各种物质的活度,当参与反应的物质是气态时,则以逸度f代替活度,在气体压力较低时,可用气体的压力代替逸度;vi和vj为电池反应式中各种物质前的计算系数。 n为电池反应中电子转移数;F为法拉第常数;R为气体常数;T为热力学温度。
此式由W.H.能斯脱在1889年从热力学导出。式中E°为电池的标准电动势,即参与电池反应物质的活度均为 1时电池的平衡电势或电动势;П为连乘符号;ai和aj分别为电池反应式中反应物一边和生成物一边的各种物质的活度,当参与反应的物质是气态时,则以逸度f代替活度,在气体压力较低时,可用气体的压力代替逸度;vi和vj为电池反应式中各种物质前的计算系数。 n为电池反应中电子转移数;F为法拉第常数;R为气体常数;T为热力学温度。例如电池Pt|H2(气,p)|HCl(a)|AgCl|Ag(固)(p为压力;a为活度)的反应式为:
H2+2AgCl─→2HCl+2Ag由于Ag和AgCl为纯固相,它们的活度应为1,因此,
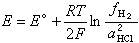 当H2压力较低时,
当H2压力较低时,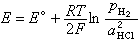 由于电池的电势是它的两个电极电势之差,得出:
由于电池的电势是它的两个电极电势之差,得出: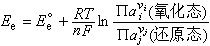 式中E懣为标准平衡电极电势(或标准电极电势), 即参与电极反应物质的活度均为1的电极电势,例如Zn|Zn2+(a)电极的电极反应式为:
式中E懣为标准平衡电极电势(或标准电极电势), 即参与电极反应物质的活度均为1的电极电势,例如Zn|Zn2+(a)电极的电极反应式为:Zn─→Zn2++2e其电极平衡电势为: