过氧化钠(卷名:化学)
sodium peroxide
化学式Na2O2。 淡黄色粉末; 熔点约675℃,密度2.805克/厘米3;易潮解。应密封保存。过氧化钠有二水合物和八水合物。
性质 过氧化钠是常用的强氧化剂。在碱性溶液中,它可以把As(Ⅲ)氧化成As(Ⅴ)化合物,把Cr(Ⅲ)氧化成Cr(Ⅵ)化合物。在高温下还可氧化分解某些岩石矿物。例如分析铬铁矿中的铁时,由大量Cr(Ⅲ)的颜色引起的干扰,可用下列方法消除:用Na2O2在600~700℃高温下将铬铁矿中Cr(Ⅲ)氧化成Na2CrO4,再用水溶掉Na2CrO4:
2Fe(CrO2)2+7Na2O2─→Fe2O3+4Na2CrO4+3Na2O
过氧化钠在潮湿空气中能吸收二氧化碳,放出氧气:
2Na2O2+2CO2─→2Na2CO3+O2因此过氧化钠可用作二氧化碳吸收剂和供氧剂。过氧化钠遇水,在低温下生成过氧化氢,在室温下放出氧气:
Na2O2+2H2O
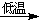 H2O2+2NaOH
H2O2+2NaOH2Na2O2+2H2O
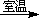 4NaOH+O2如果将过氧化钠溶于冰冷的硫酸中,再减压蒸馏可得过氧化氢:
4NaOH+O2如果将过氧化钠溶于冰冷的硫酸中,再减压蒸馏可得过氧化氢:Na2O2+H2SO4
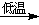 H2O2+Na2SO4
H2O2+Na2SO4过氧化钠粉末易使皮肤灼伤,与易燃物接触,会引起着火,高温下与有机物接触,会发生爆炸。由过氧化钠引起的火灾必须用盐或沙扑灭,不能用水。
制法 钠在空气中燃烧的主要产物是过氧化钠, 但要制得纯品须严格控制条件。工业上是先将金属钠熔化,通入定量的不含二氧化碳的干空气,维持180~200℃温度,钠就氧化成氧化钠Na2O,再增加气量,并升温至300~400℃,即得纯净的Na2O2。
应用 过氧化钠在纺织和造纸工业上用作漂白剂,在分析化学上用于处理矿样。