熵(卷名:物理学)
entropy
热力学系统的一个重要的态函数。熵的变化指明了自发过程进行的方向,并可给出孤立系统达到平衡的必要条件。因此,它是热力学第二定律的简明概括。
热力学意义 一个实际过程除了必须遵守能量守恒以外,还有一个能量转换和传递的方向问题。人们期望有一个普适判据来判断自发过程的方向。根据热力学第二定律概括的关于热力学过程单向性的经验,自发过程的方向决定于系统初态和终态的差异。因此,应该可以找到一个决定于系统状态的物理量,用它的变化来表述自发过程的方向。1854年,R.克劳修斯首先找到了这样一个物理量,1865年,他给这个物理量正式定名为熵。
 克劳修斯在研究卡诺热机(见卡诺循环)时,根据卡诺定理得出,对任意循环过程都有
克劳修斯在研究卡诺热机(见卡诺循环)时,根据卡诺定理得出,对任意循环过程都有 ,婾Q为系统从温度为 T的热源所吸收的热量,等号对应可逆过程,不等号对应不可逆过程。上式称为克劳修斯不等式。如果过程是可逆的,上式中的T也是系统的温度,因为可逆过程中热源与系统的温度相同。
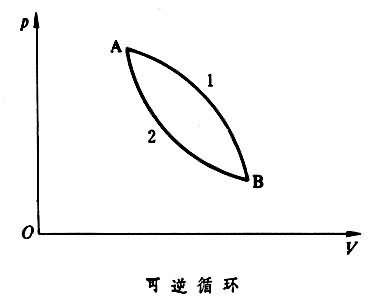
,婾Q为系统从温度为 T的热源所吸收的热量,等号对应可逆过程,不等号对应不可逆过程。上式称为克劳修斯不等式。如果过程是可逆的,上式中的T也是系统的温度,因为可逆过程中热源与系统的温度相同。若系统从初态A经可逆过程"1"变到未态B,又经任意另一可逆过程"2"回到初态A,构成一个可逆循环,如图所示。则对可逆循环有:
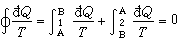 或
或 。由于过程"1"、"2"是任意的,所以积分
。由于过程"1"、"2"是任意的,所以积分 的值与状态A、B之间经历的过程无关,完全由初态A和终态B决定,因此被积函数应当是一个状态函数的全微分,即T-1是婾Q的积分因子。这一状态函数称为熵,以符号S表示。则
的值与状态A、B之间经历的过程无关,完全由初态A和终态B决定,因此被积函数应当是一个状态函数的全微分,即T-1是婾Q的积分因子。这一状态函数称为熵,以符号S表示。则 或
或 。可见熵是广延量,单位为J/K。
。可见熵是广延量,单位为J/K。对于不可逆过程,根据熵的定义及克劳修斯不等式,有
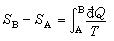 ,对于不可逆微变化过程,有
,对于不可逆微变化过程,有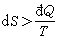 。可见,在可逆微变化过程中,熵的变化等于系统从热源吸收的热量与热源的热力学温度(见热力学温标)之比,在 不可逆微变化过程中,这个比小于熵的变化。这是热力学第二定律的直接结果和概括,是热力学第二定律的数学表达式。
。可见,在可逆微变化过程中,熵的变化等于系统从热源吸收的热量与热源的热力学温度(见热力学温标)之比,在 不可逆微变化过程中,这个比小于熵的变化。这是热力学第二定律的直接结果和概括,是热力学第二定律的数学表达式。对于绝热过程,婾Q=0,因而dS≥0。即系统经绝热过程由一态到达另一态时,系统的熵永不减少(熵在可逆绝热过程中不变,在不可逆绝热过程中增加)。此结论称为熵增加原理。如果系统是孤立的,其内部一切变化与外界无关,必然是绝热过程。所以熵增加原理的一个通常说法是,“一个孤立系统的熵永不会减少”。在后一种说法里,孤立系统的熵必然包括非平衡态的熵。因为一个孤立系统在变化的时候,不可能处在平衡态。根据熵的广延性质,非平衡态的熵可定义为处在局域平衡的各部分的熵之和。
根据熵增加原理,孤立系统越接近平衡态,其熵值越大。当系统的熵达到最大值时,系统达到平衡态,过程不再进行,只要没有外界作用,系统将始终保持平衡态。因此,可由孤立系统熵的变化来判断系统中过程进行的方向,只有dS≥0的过程才是允许的。可以证明熵增加原理与热力学第二定律的开氏、克氏等表述等效。实质上,熵增加原理就是热力学第二定律。如果系统从平衡态有一微小变动,系统熵的变化 δS必小于零。因此,δS<0是判定孤立系统是否达到平衡的条件。熵或熵的变化不仅能判断过程进行的方向,还反映该系统所处状态的稳定情况。
微观解释 L.玻耳兹曼首先建立了熵与系统微观性质的联系,从而使熵这个抽象概念的物理意义得到深入的解释。以k代表玻耳兹曼常数,W 代表某一宏观态所对应的微观态的数目(或称热力学概率),则熵的统计表达式为
 ,式中So为熵常数。当把So选为零时,得到玻耳兹曼关系
,式中So为熵常数。当把So选为零时,得到玻耳兹曼关系 因此,可以把熵看作是与系统状态无序程度相联系的量。系统无序程度越高,即系统越"混乱",其对应的微观态数目越多,熵就越大;反之系统越有序,熵就越小。
因此,可以把熵看作是与系统状态无序程度相联系的量。系统无序程度越高,即系统越"混乱",其对应的微观态数目越多,熵就越大;反之系统越有序,熵就越小。1927年J.冯·诺埃曼用密度算符(见统计物理学)给出了熵的量子力学表述,称冯·诺埃曼公式
 假定体系在确定的密度算符ρ所描述的状态下,具有W 个不同的纯态,各态都以相等的概率出现,即
假定体系在确定的密度算符ρ所描述的状态下,具有W 个不同的纯态,各态都以相等的概率出现,即 ,则有
,则有 ,即玻耳兹曼关系。可见,量子系统混合态中包含的纯态数越多,熵越大。所以,熵又是体系无序度的量度。
,即玻耳兹曼关系。可见,量子系统混合态中包含的纯态数越多,熵越大。所以,熵又是体系无序度的量度。在其他领域中的应用 熵的应用不限于热力学、统计物理学的范畴。1948年C.E.香农将熵的概念同信息论联系了起来。他认为熵是概率分布P1=P2=,...,=PN的函数,他定义熵为
 PK是事件出现第K 种情况的概率,满足
PK是事件出现第K 种情况的概率,满足 C是大于零的实数。可见,在信息论中可以用熵作为某事件不确定度的量度,信息量越大,体系的结构越有规则,功能越完善,熵就越小;信息量越小,体系的不确定度越大,熵就越大。信息量就是负熵。这样,便可对信息的计量、传递、变换和存储进行理论研究。此外,熵在控制论、概率论、数论、天体物理学乃至生命科学等领域,也都有一定的应用。
C是大于零的实数。可见,在信息论中可以用熵作为某事件不确定度的量度,信息量越大,体系的结构越有规则,功能越完善,熵就越小;信息量越小,体系的不确定度越大,熵就越大。信息量就是负熵。这样,便可对信息的计量、传递、变换和存储进行理论研究。此外,熵在控制论、概率论、数论、天体物理学乃至生命科学等领域,也都有一定的应用。