量子数(卷名:化学)
quantum number
表示原子内电子运动的能量、角动量、……等的一组整数或半整数。按量子力学原理,原子中核外电子运动、状态、角动量都不是连续变化的,而是跳跃式变化的,即量子化的。量子数有主量子数、角量子数、磁量子数和自旋量子数。
主量子数 确定核外电子运动能量的主要量子数,用n表示,它们的取值是:n=1,2,3,4,…。电子能层为第1(K)、第2(L)、第3(M)、第4(N)、……。氢原子内电子在各能层的能量为:
En=-13.6/n2 (eV)n=1,氢原子内电子在第一能层的能量为-13.6电子伏;n=2,氢原子内电子在第二能层的能量为-3.4电子伏;……;n愈大,能量愈高。
角量子数 表示轨道角动量的量子数。角动量用Μl表示:
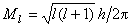 角量子数用l表示,取值为0,1,…,n-1,h为普朗克常数。l值表示原子轨道或电子云的形状。l=0,原子轨道或电子云是球形对称的;n=2,l=1,电子云是无把哑铃形;n=3,l=2,电子云为花瓣形;l=3的电子云形状更为复杂。光谱学上以 s、p、d、f、…分别表示l=0,1,2,3,…,如n=4,l=0、1、2、3,分别以4s、4p、4d、4f表示。或者说,l表示同一电子能量中的分层。各分层能量高低的关系如下:l值相同而n值不同,则E1S<E2S<E3S;n值相同而l值不同,则E4S<E4P<E4d<E4f。从能量角度看,一个分层代表一个能级。
角量子数用l表示,取值为0,1,…,n-1,h为普朗克常数。l值表示原子轨道或电子云的形状。l=0,原子轨道或电子云是球形对称的;n=2,l=1,电子云是无把哑铃形;n=3,l=2,电子云为花瓣形;l=3的电子云形状更为复杂。光谱学上以 s、p、d、f、…分别表示l=0,1,2,3,…,如n=4,l=0、1、2、3,分别以4s、4p、4d、4f表示。或者说,l表示同一电子能量中的分层。各分层能量高低的关系如下:l值相同而n值不同,则E1S<E2S<E3S;n值相同而l值不同,则E4S<E4P<E4d<E4f。从能量角度看,一个分层代表一个能级。磁量子数 表示轨道角动量方向量子数沿磁场的分量:
Μz=mh/2πm为磁量子数,取值为0,±1,±2,…,±l,共有2l+1个取值。n=2,l=0,m=0,表明只有一个轨道,即2s;n=2,l=1,m=0,±1,表示有三个空间取向不同的轨道,即2px、2py、2pz。无外加磁场时,三个轨道的能量相同;有外加磁场时,因三个轨道在磁场中的取向不同,表现出较小的能量差别,所以某些线状光谱分裂成几条。
自旋量子数 决定电子自旋运动的角动量沿着磁场的分量:
Μs=msh/2πms为自旋量子数,取值为±1/2,表明一个轨道上最多只能容纳自旋反向的两个电子。